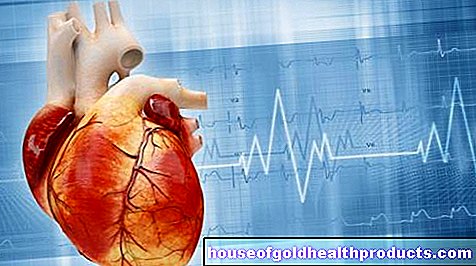
קוצב לב במוח מאט את פרקינסון המוקדם
כריסטיאן פוקס למדה עיתונאות ופסיכולוגיה בהמבורג. העורך הרפואי המנוסה כותב מאז 2001 מאמרי מגזין, חדשות וטקסטים עובדתיים על כל נושאי הבריאות שאפשר להעלות על הדעת. בנוסף לעבודתה ב-, כריסטיאנה פוקס פעילה גם בפרוזה. רומן הפשע הראשון שלה יצא לאור בשנת 2012, והיא גם כותבת, מעצבת ומפרסמת מחזות פשע משלה.
פוסטים נוספים של Christiane Fux כל תוכן נבדק על ידי עיתונאים רפואיים.גירוי מוחי עמוק (DBS) משמש כיום רק במחלת פרקינסון בשלב מאוחר - כאשר התרופה כבר אינה יעילה או בעלת תופעות לוואי חמורות. כעת הוכח כי לשיטה יכולה להיות אפילו פוטנציאל להאט את המחלה בשלב מוקדם.
לגירוי מוחי עמוק, המטופל נטוע באלקטרודות קטנות באזורים ספציפיים מאוד במוח. הדחפים החשמליים הדרושים מגיעים ממכשיר המונח מתחת לעצם הבריח, בדומה לקוצב לב. התוצאה לרוב מעוררת השתאות: בחולים שבקושי יכלו לנוע בשטף, היו להם קשיי דיבור וסבלו מרעידות בזמן מנוחה (רעד), הסימפטומים לפעמים משתפרים באופן דרמטי.
קוצב לב בשלב מוקדם
כעת חוקרים מאוניברסיטת ונדרבילט בדקו גירוי מוחי עמוק בחולי פרקינסון בשלב מוקדם של המחלה. הם גייסו בסך הכל 30 משתתפים לניסוי שלהם - סוכנות המזון והתרופות האמריקאית (FDA) לא אישרה להם יותר נבדקים. מכיוון שההתערבות במוח בקרב יותר חולים עם תסמינים קלים יחסית לא נראתה בתחילה מוצדקת מבחינה אתית.
פחות רעידות
התוצאה: תוך שנתיים, 86 אחוזים מהמשתתפים שקיבלו רק תרופות פיתחו רעד בגפיים נוספות. בקבוצה עם קוצב לב נוסף במוח, זה היה רק 46 אחוזים. בארבעה מהם הרעידה אפילו השתפרה, בחולה אחד היא נעלמה כליל.
"נראה כי גירוי מוחי עמוק יכול להאט את התקדמות הרעידות בפרקינסון בשלב מוקדם", אמר דייויד צ'ארלס, מחבר בכיר של המחקר. "זה מדהים, כי עד כה אין טיפול שמאט את כל היבט של המחלה."
החולים שהשתתפו היו בני 50 עד 75 שנים בתחילת המחקר. בשלב זה נטלת תרופות לפרקינסון במשך שישה חודשים לפחות וארבע שנים לכל היותר. המשתתפים נפגשו לבדיקות נוירולוגיות כל שישה חודשים. על מנת לקבוע את מצבם הנוכחי של החולים בצורה המדויקת ביותר האפשרית, הם עברו שלב שטיפה של שבוע לפני הבדיקות, שבמהלכו לא קיבלו תרופות וללא גירוי מוחי עמוק.
ההשפעה עדיין לא ידועה
עדיין לא נחקר כיצד בדיוק פועל DBS. עם זאת ההנחה היא שהדחפים החשמליים מעכבים אזורי מוח מופעלים יתר על המידה. ההליך משמש גם לטיפול במחלות נוירולוגיות ופסיכיאטריות אחרות, כולל אפילפסיה, הפרעה אובססיבית-כפייתית ודיכאון חמור שלא משתפר עם טיפול תרופתי או פסיכותרפויטי.
המדענים רוצים כעת לחזור על הניסוי בשנת 2019 עם קבוצה של כ -280 חולי פרקינסון. לאור מחקר הפיילוט המוצלח, ה- FDA אישר כעת את מספר המשתתפים הגדול בהרבה.
מחסור בדופמין במוח
במחלת פרקינסון התאים המייצרים דופמין בחומר השחור במוח מתים באופן הדרגתי. חומר השליח נחוץ, בין היתר, לתיאום תנועות. רק כאשר יותר ממחצית התאים מתו מופיעים התסמינים הראשונים של פרקינסון. אלה כוללים רעידות, תנועות האטות, התקשות שרירים, הבעות פנים נוקשות, הליכה לא יציבה והפרעות בדיבור.
200 אלף חולי פרקינסון בגרמניה
לאחר מכן תרופות המכילות לבודופה עוזרות בין היתר. הוא הופך לדופמין בתאי העצב. אולם בטווח הארוך תופעות הלוואי כמו טלטלות בלתי רצוניות ותנועות קשות עולות, והתרופה הופכת פחות יעילה. אז גירוי מוחי עמוק הוא אופציה.
בסביבות 220 אלף בני אדם חיים עם המחלה בגרמניה. זה בדרך כלל מתחיל בין הגילאים 50-60. עם זאת, כל אדם עשירי שנפגע חולה לפני גיל 40.
none: gpp לעשן הַפסָקַת וֶסֶת